Imaging of Matter
Ultrakurze optische und Röntgenpulse spüren flüchtiges Zwischenprodukt in der Katalyse auf
29. Mai 2024
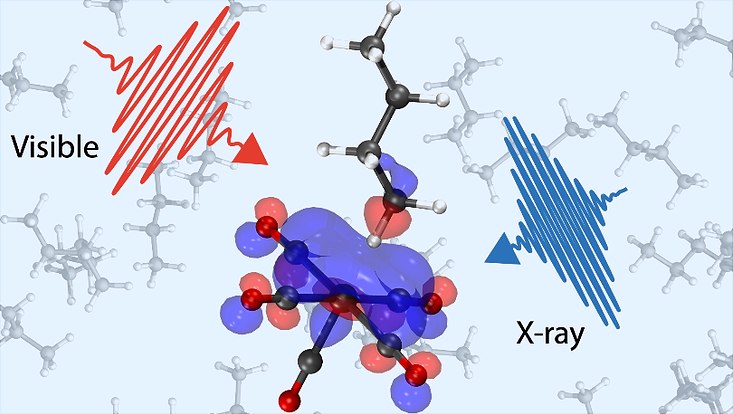
Foto: Raphael Jay
Ein internationales Forschungsteam hat mit Hilfe von sichtbarem Licht und Röntgenstrahlen die Bildung einer wichtigen Molekülstruktur aufgeklärt, die entsteht, bevor die Bindung zwischen einem Kohlenstoff- und einem Wasserstoffatom aufgebrochen werden kann. Die im „Journal of the American Chemical Society“ (JACS) veröffentlichte Studie nutzt eine Kombination spektroskopischer Methoden, um Fragen zu klären, die seit 50 Jahren diskutiert werden, und deren Beantwortung helfen kann, Katalysatoren besser zu machen.
Die Umwandlung des Treibhausgases Methan und längerkettiger Alkane in weniger schädliche Chemikalien ist eine der großen Herausforderungen der Chemie. Solche Umwandlungen erfordern das Aufbrechen von Kohlenstoff-Wasserstoff-Bindungen (C-H), die zu den stärksten chemischen Bindungen in der Natur gehören. Eine Möglichkeit, C-H-Bindungen zu brechen, sind Metallkatalysatoren. Vor mehr als fünfzig Jahren fand man heraus, dass C-H-Bindungen brechen, wenn solche Katalysatoren in Alkanlösungen mit sichtbarem Licht beleuchtet werden. Wichtige Details waren jedoch bis heute ungeklärt: Was genau passiert, nachdem die Katalysatoren durch Licht aktiviert wurden? Wie nähern sich die Alkanmoleküle den Metallkatalysatoren? Und wie binden sie sich dann an den Katalysator?
Einem internationalen Team unter der Leitung von Forschenden der Universität Uppsala in Zusammenarbeit mit Forschenden der Universität Hamburg, der Universität Stockholm, des Max-Born-Instituts und des Helmholtz-Zentrums Berlin (HZB) ist es nun gelungen, diese Fragen mit einer Kombination aus Röntgenlicht und sichtbarem Licht zu beantworten. Da eine C-H-Bindung durch Andocken eines Alkans an das Metallatom in einer sogenannten C-H-Aktivierungsreaktion aufgebrochen werden kann, ist es wichtig, diesen Prozess in allen Einzelheiten zu verstehen.
Katalysator wird innerhalb von weniger als 100 Femtosekunden aktiviert
In zwei Experimenten, eines im Laserlabor der Huse-Gruppe an der Universität Hamburg und eines am Synchrotron BESSY II am HZB, konnte das Team verfolgen, wie ein Metallkatalysator aus Chrom zunächst durch ultraviolettes Licht aktiviert wird und dann ein Alkan aus der umgebenden Lösung bindet. Mit ultrakurzen optischen Pulsen sowie Röntgenpulsen der Synchrotronstrahlungsquelle BESSY II konnte die Reaktion von der Aktivierung über die Abkühlung bis zur Alkanbindung ans Chromzentrum verfolgt werden. Die Messungen ergaben, dass das anfängliche „Einschalten“ des Katalysators innerhalb von weniger als 100 Femtosekunden (0,0000000000001 Sekunden) erfolgt. In diesem Zustand ist der Katalysator sehr heiß und seine Teile oszillieren um das Chromzentrum. Erst wenn diese Schwingungen abgeklungen sind, kann sich das Alkanmolekül dem Katalysator nähern und an sich ihn in einer Konfiguration binden, die als σ-Komplex bezeichnet wird, und deren Bildung etwa 8 Pikosekunden (0,000000000008 Sekunden) dauert.
„Die Beobachtung des Prozesses mit optischen Lichtblitzen und Röntgenpulsen ermöglichte es uns, ein vollständiges Bild des Prozesses zu bekommen. Wir haben dazu Licht in kurze Lichtblitze „verpackt“, um in einer Sequenz kurz aufeinander folgender Schnappschüsse die Reaktionen zu verfolgen. Die optischen Pulse waren so kurz, dass wir selbst die schnellsten atomaren Bewegungen auf dem Weg zum σ-Komplex erfassen konnten. Mit Röntgenstrahlen haben wir dann detailliert abgetastet, auf welche Weise sich die Bindung zwischen dem Metall und dem Alkan bildet", erklärt Raphael Jay, Forscher an der Universität Uppsala und leitender Experimentator der Studie.
„Die optische Spektroskopie ist eine der ältesten wissenschaftlichen Methoden zur Verfolgung chemischer Reaktionen. Dennoch verbessern Wissenschaftlerinnen und Wissenschaftler ihre Messinstrumente ständig, sodass jetzt auch kleine Details sichtbar gemacht werden können, die Schlüsselinformationen darüber liefern, wie der Chromkomplex zu einem σ-Komplex wird. Aber keine Methode liefert die ganze Wahrheit, verschiedene Augen sehen verschiedene Dinge. Deshalb haben wir zwei Methoden mit unterschiedlichen Stärken eingesetzt, um lange bestehende Fragen zur σ-Komplexbildung zu beantworten", ergänzt Nils Huse, Professor für Physik an der Universität Hamburg und Forscher im Exzellenzcluster „CUI: Advanced Imaging of Matter“. Um die komplexen experimentellen Daten zu modellieren und zu interpretieren, führten zudem Theoretiker der Universität Uppsala und der Universität Stockholm moderne quantenchemische Berechnungen durch.
Die Studie klärt nun eindeutig, was seit fünfzig Jahren vermutet wurde, nämlich wie sich σ-Komplexe im Detail bilden und wie sie die C-H-Bindungen von Alkanen in Aktivierungsreaktionen abschwächen.
Mit ihrer Kombination von Methoden wollen die Forschenden als Nächstes verstehen, wie die Struktur des Katalysators und das spezifische Metallelement im Zentrum des Katalysators die Art und Weise beeinflussen, wie der Katalysator aktiviert wird und wie er mit Alkanen interagiert. Dadurch könnte es möglich werden, das Verhalten des Katalysators bei Aktivierungsreaktionen von C-H-Bindungen besser zu steuern und anzupassen. Text: Universität Uppsala, red.
Originalpubliklation
R. M. Jay, M. R. Coates, H. Zhao et al.
„Photochemical Formation and Electronic Structure of an Alkane σ-Complex from Time Resolved Optical and X-ray Absorption Spectroscopy“
J. Am. Chem. Soc. 146, 20, 14000–14011 (2024)